细胞治疗是指利用患者自体(或异体)的成体细胞(或干细胞)对组织、器官进行修复的治疗方法,广泛用于骨髓移植、晚期肝硬化、股骨头坏死、恶性肿瘤、心肌梗死等疾病。作为近年来肿瘤等严重疾病治疗的主流发展方向,是血液系统疾病、肿瘤疾病等精准治疗的热门技术。针对血液系统疾病,可以通过对造血干/祖细胞的增殖、分化和调控进行治疗;针对肿瘤疾病,则可以通过在体外对各种治疗细胞如干细胞、间充质细胞、淋巴细胞等进行处理,使其活化为对肿瘤有杀伤作用的免疫活性细胞,然后注回患者体内发挥治疗作用。
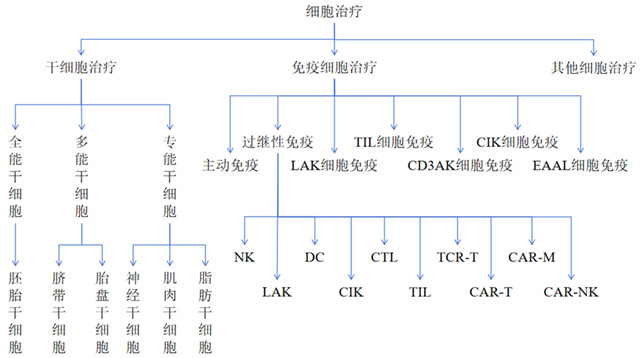
细胞治疗主要分为三大类:干细胞治疗、免疫细胞治疗和其他细胞治疗,干细胞治疗主要包括全能干细胞、多能干细胞、专能干细胞;免疫细胞治疗则主要包括主动免疫、过继性免疫等。目前,常用的免疫细胞疗法包括非特异性免疫疗法(LAK、CIK以及NK等)以及特异性免疫疗法(TIL、CAR-T以及TCR-T等)。
二、不同来源细胞的可专利性
2.1 人类胚胎
中华人民共和国专利法(2020年修正)第5条规定:对违反法律、社会公德或者妨害公共利益的发明创造,不授予专利权。
无论是人类胚胎本身,还是从人类胚胎中分离获取任何细胞的方法,都属于审查指南举例中的人类胚胎的工业或商业目的的应用,是不授予专利权的客体。在实际审查过程中,通常对人胚胎做广义的定义,即从受精卵开始到新生儿出生前任何阶段的胚胎,包括卵裂期、桑葚期、囊胚期、着床期、胚层分化期的胚胎等。关于人胚胎来源,也做广义解释,包括体外受精多余的囊胚、体细胞核移植技术所获得的囊胚、自然或自愿选择流产的胎儿等任何来源的胚胎。
2.2 胚胎干细胞或全能干细胞
干细胞可根据个体发育过程分为胚胎干细胞和成体干细胞;或根据干细胞分化的能力分为全能干细胞、多能干细胞和专能干细胞,“胚胎干细胞”和“全能干细胞”来自两种不同的分类方法。“胚胎干细胞”从早期胚胎(原肠胚期之前)或原始性腺中分离得到,其制备过程必然涉及人类胚胎的使用,因此也属于不授予专利权的客体。而“全能干细胞”或“多能干细胞”,如果其制备过程并未使用人类胚胎,则具有授予专利权的前景。
2.3 诱导性多能干细胞
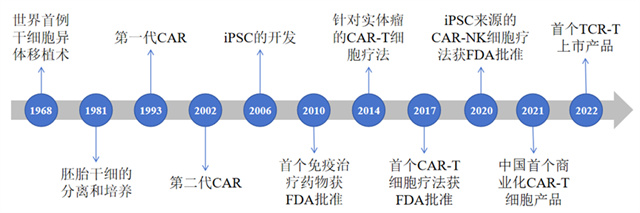
诱导性多能干细胞(induced pluripotent stem cell,iPSC)是指通过导入特定的转录因子将终末分化的体细胞重编程为多能性干细胞。2006年日本科学家率先公开了诱导多能干细胞的研究,将Oct3/4、Sox2、c-Myc和Klf4四种转录因子基因克隆入病毒载体,然后引入小鼠成纤维细胞,发现可诱导其发生转化,产生的iPSC在形态、基因和蛋白表达、表观遗传修饰状态、细胞倍增能力、类胚体和畸形瘤生成能力、分化能力等方面都与胚胎干细胞相似,但不再利用胚胎细胞或卵细胞,成功避开了胚胎干细胞技术的伦理限制。2008年9月,诱导多能干细胞技术专利在日本首次获得授权,随后欧美等多国专利局也相继授权多个iPSC相关专利。
三、细胞治疗相关专利申请
3.1 细胞治疗相关专利的可专利性技术点
如前文所述,在细胞治疗相关的专利申请中,干细胞的制备、免疫细胞的制备、靶点的选择、抗体的选择、CAR的设计、CAR的制备等均可作为申请专利的主题。
就靶点而言,既可以针对新发现的靶点进行专利申请,也可以针对已知靶点的新作用进行专利申请。例如CN108047333B,公开了一种以CD33为靶点的特异性抗体、CAR-NK细胞及其制备和应用,在权利要求1中限定了抗CD33抗体的重链可变区和轻链可变区的互补决定区的序列,于2021年5月25日获得授权。




相比较于化学药,免疫细胞治疗技术相关生物药产品类专利申请由于被仿制的难度更大,技术方案的非显而易见性较强,技术效果难以预期,在技术方案尚未被公开时难以被抢占申请,因此很多申请人并不会争取尽早申请专利。相反,为了获得更长的专利保护期,申请人倾向于较晚地提交专利申请,例如在临床项目以前再申请专利。
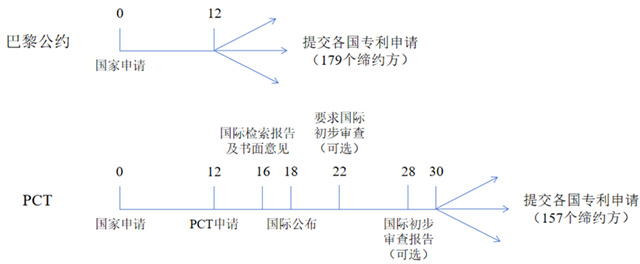
同时,为了获得更广阔的发展空间和更丰厚的利润,众多国内医药企业纷纷选择开辟海外新市场,因此海外专利申请也是必不可少的保护措施。海外专利申请有巴黎公约和PCT两种途径,申请人可以根据企业自身情况和不同的目标国家进行选择。
四、案例分析
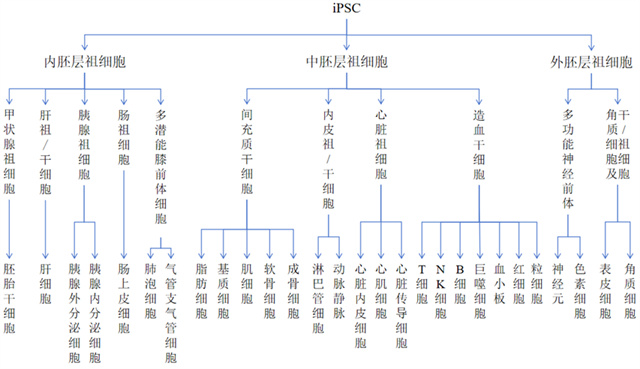
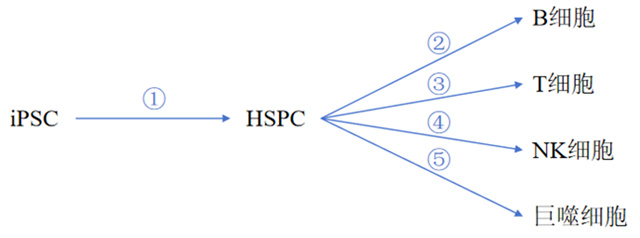
如前所述,针对使用iPSC分化得到的不同细胞,可以先对iPSC进行遗传修饰,再将其分化为不同的细胞。同理,在有关不同细胞的制备方法的专利申请中,其发明点可以在于靶细胞的某种特殊修饰,也可以仅在于对iPSC的遗传修饰、或iPSC的制备方法、或诱导iPSC分化为某种前体细胞的方法。
案例1:一种制备B细胞的方法,包括:
诱导iPSC分化为HSPC(步骤①),再诱导所述HSPC分化得到B细胞(步骤②)。
案例2:一种制备T细胞的方法,包括:
诱导iPSC分化为HSPC(步骤①),再诱导所述HSPC分化得到T细胞(步骤③)。
其中步骤①与案例1相同,步骤③为常规的T细胞分化方法。
案例3:一种制备自然杀伤细胞的方法,包括:
诱导iPSC分化为HSPC(步骤①),再诱导所述HSPC分化得到NK细胞(步骤④)。
其中步骤①与案例1相同,步骤④为常规的NK细胞分化方法。
案例4:一种制备巨噬细胞的方法,包括:
诱导iPSC分化为HSPC(步骤①),再诱导所述HSPC分化得到巨噬细胞(步骤⑤)。
其中步骤①与案例1相同,步骤⑤为常规的巨噬细胞分化方法。
由此可见,案例1-4实际上都是诱导iPSC分化为不同细胞的方法,并且发明点都在于诱导iPSC分化为HSPC这一步骤。尽管如此,由于案例1-4请求保护的是不同细胞的制备方法,因此在实际审查过程中,案例1-4陆续全部获得了授权。
五、小结
综上所述,在细胞治疗领域中具有可专利性的技术点很多,需要注意区分不能被授予专利权的客体,例如疾病的诊断和治疗方法、人类胚胎和从人类胚胎中分离获取任何细胞的方法等。同时需要综合考虑自身研究进展、相关研究领域的发展情况、不同专利申请方式的审查周期等,选择合适的专利申请时间和国家。
公司简介
锦尚知识产权代理事务所专注于高价值专利,坚定为优质、创新性企业提供全球化知识产权服务、致力于为国内外创新主体提供高端专业化知识产权解决方案和知识产权法律保护服务,为客户的创新成果保驾护航,为企业的长足发展锦上添花。

欢迎大家加入锦尚实务交流群,交流知识产权实务问题,分享实务知识。






 0512-65090998
0512-65090998
